Oral L-ornithine L-aspartate in minimal hepatic encephalopathy: A randomized, double-blind, placebo-controlled trial.
Alvares-da-Silva MR, Araujo A, Vicenzi JR et al.
Hepatol Res 2014; 44(9): 956-63
Interwencja terapeutyczna
Parametry oceny
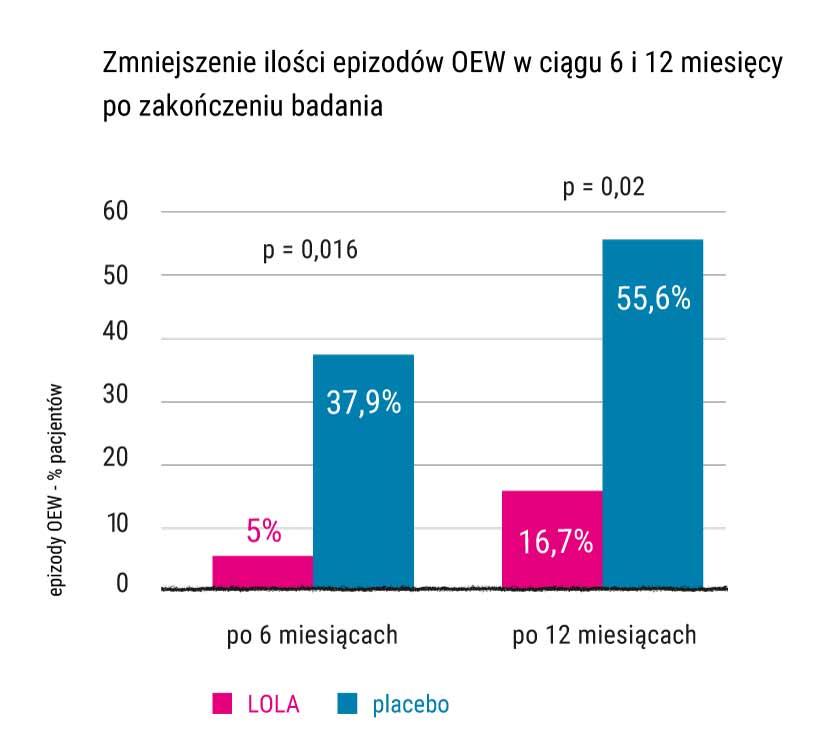
Wyniki badania
W grupie pacjentów otrzymujących L-ornityny L-asparaginian (LOLA):